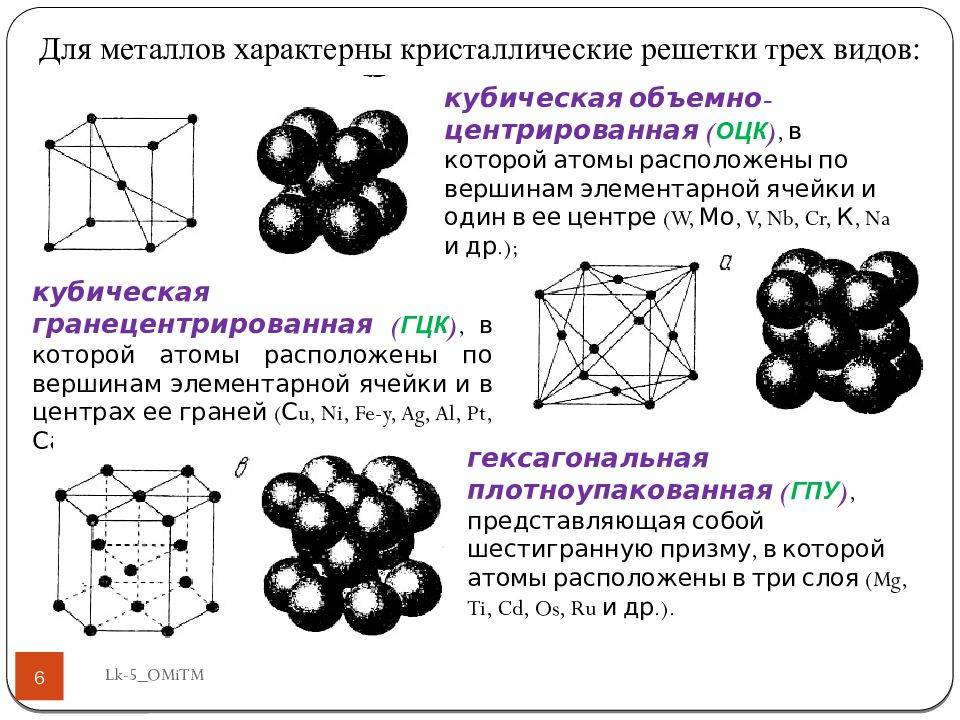
Виды кристаллических решеток металлов

В огромном ряду материалов, с незапамятных времен известных человеку и широко используемых им в своей жизни и деятельности, металлы всегда занимали особое место.
Подтверждение этому: и в названиях эпох (золотой, серебряный, бронзовый, железный века), на которые греки делили историю человечества: и в археологических находках металлических изделий (кованые медные украшения, сельскохозяйственные орудия); и в повсеместном использовании металлов и сплавов в современной технике. Причина этого — в особых свойствах металлов, выгодно отличающих их от других материалов и делающих во многих случаях незаменимыми.
Материаловедение. Металловедение.
Металлы – один из классов конструкционных материалов, характеризующийся определенным набором свойств:
- «металлический блеск» (хорошая отражательная способность);
- пластичность;
- высокая теплопроводность;
- высокая электропроводность.
Строение металлов. Атомно-кристаллическое строение металлов
Данные свойства обусловлены особенностями строения металлов.
Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбиталям вращаются электроны.
На последнем уровне число электронов невелико и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов.
Дефекты кристаллического строения. Точечные дефекты.Аллотропия. Полиморфные превращения. Магнитные превращения.
Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Кристаллическая решетка металлов
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка. Другими словами, кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело.
Элементарная ячейка – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл. Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются:
- размеры ребер элементарной ячейки. a, b, c – периоды решетки – расстояния между центрами ближайших атомов (в одном направлении выдерживаются строго определенными);
- углы между осями (α, β, χ);
- координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке;
- базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки;
- плотность упаковки атомов в кристаллической решетке – объем, занятый атомами, которые условно рассматриваются как жесткие шары. Ее определяют как отношение объема, занятого атомами к объему ячейки (для объемно-центрированной кубической решетки – 0,68, для гранецентрированной кубической решетки – 0,74).
Схема кристаллической решетки
Рис. 1
Классификация возможных видов кристаллических решеток была проведена французским ученым О. Браве, соответственно они получили название «решетки Браве». Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа:
- примитивный – узлы решетки совпадают с вершинами элементарных ячеек;
- базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях;
- объемно-центрированный – атомы занимают вершины ячеек и ее центр;
- гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней.
Кристаллическое строение металлов
Определение 1
Металлы – это группа элементов периодической таблицы Менделеева, которые являются восстановителями с положительной степенью окисления, обладают твердостью, пластичностью и упругостью, обусловленными их кристаллическим строением.
Кристаллические решетки металлов представляют собой атомы, упорядоченные определенным образом. В состав каждого атома входят несколько отрицательно заряженных электронов и положительно заряженное ядро. Атомы металлов мало электронов, поэтому они являются ионами. Единица кристаллической решетки представляет собой элементарную кристаллическую ячейку, в гранях и узлах которой находятся ионы. Вместе их удерживают металлические связи, которые возникают в результате беспорядочного движения отделившихся от атомов электронов. Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны.
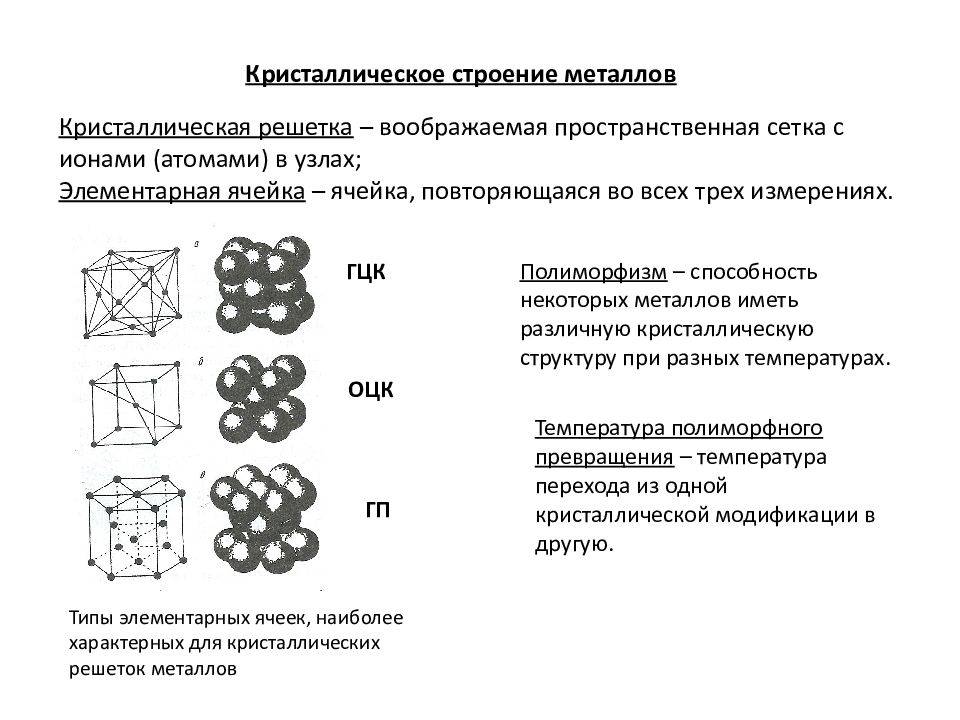
Подавляющему большинству металлов свойственно образование высокосимметричных кристаллических решеток с плотной упаковкой атомов. Самыми распространенными типами кристаллических решеток атомов являются:
- Объемно-центрированная кубическая кристаллическая решетка, которая представляет собой куб с дополнительными атомами, которые находятся в центре. Такая решетка имеется у железа, хрома, вольфрама, молибдена и ванадия.
- Гранецентрированная кубическая кристаллическая решетка, которая представляет собой куб с дополнительными атомами, находящиеся центре каждой грани. Такая решетка имеется у железа, алюминия, меди, никеля, а также золота.
- Гексагональная плотноупакованная кристаллическая решетка с шестиугольниками в нижнем и верхнем основаниях, которые образованы расположенными там атомами, а также одним атомом в центре каждого шестиугольника. Внутри каждой фигуры находится три атома. Такая решетка имеется у кадмия, цинка, магния и других металлов.
- Тетрагональная кристаллическая решетка получается в результате растягивания куба вдоль одной оси. Данный тип решетки может быть гранецентрированным и объемноцентрированным. Такую решетку имеют радий и индий.
У некоторых видов металлов кристаллическая решетка изменяется в результате изменения температуры. Данное явления называется аллотропией или полиморфизм. Такое явления может быть причиной изменения свойств металла, а характерно оно для цинка, железа, олова и циркония.
Кристаллизация сплавов
Первичная кристаллизация – это затвердевание расплава с образованием кристаллических решеток. Пространственные атомные и молекулярные структуры, возникающие в ходе такого процесса, оказывают решающее влияние на свойства получаемого сплава. https://www.youtube.com/watch?v=BDyvsRoNG08 Сначала в остывающем расплаве возникают центры кристаллизации, вокруг них в ходе процесса и нарастают кристаллы, многократно повторяя структуру центра. В качестве центров кристаллизации могут выступать:
- Первые образовавшиеся кристаллы в зонах локального охлаждения, чаще всего у стенок литейной формы.
- Частички неметаллических примесей.
- Тугоплавкие примеси, уже находящиеся в твердой форме.
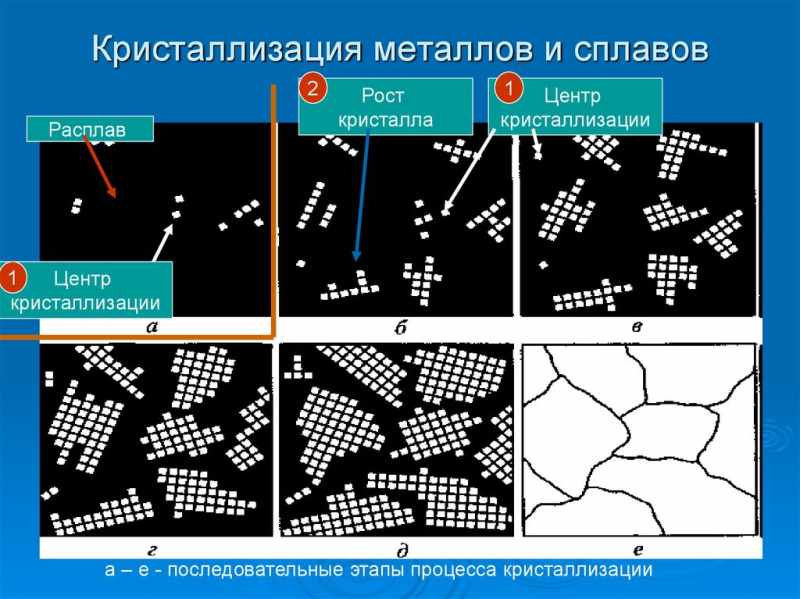 Кристаллы обычно растут в направлении роста градиента температуры. Если рост решеток не встречает физических препятствий, образуются ветвящиеся кристаллические структуры, напоминающие кораллы – дендриты. Если они растут из разных центров и встречаются в расплаве, то препятствуют росту друг друга и искажают свою форму. Такие искаженные кристаллы – это кристаллиты, или зерна. Совокупность отдельных зерен срастается в поликристаллическое тело. Отдельные кристаллиты достигают размеров от одного до 10 000 микрон и по-разному развернуты в пространстве. На стыках отдельных кристаллитов образуется граничный слой, в котором кристаллические решетки разорваны. Такие слои обладают измененными химическими и физическими свойствами.
Кристаллы обычно растут в направлении роста градиента температуры. Если рост решеток не встречает физических препятствий, образуются ветвящиеся кристаллические структуры, напоминающие кораллы – дендриты. Если они растут из разных центров и встречаются в расплаве, то препятствуют росту друг друга и искажают свою форму. Такие искаженные кристаллы – это кристаллиты, или зерна. Совокупность отдельных зерен срастается в поликристаллическое тело. Отдельные кристаллиты достигают размеров от одного до 10 000 микрон и по-разному развернуты в пространстве. На стыках отдельных кристаллитов образуется граничный слой, в котором кристаллические решетки разорваны. Такие слои обладают измененными химическими и физическими свойствами.
Решетки кристаллитов могут обладать разными дефектами структуры:
- точечные;
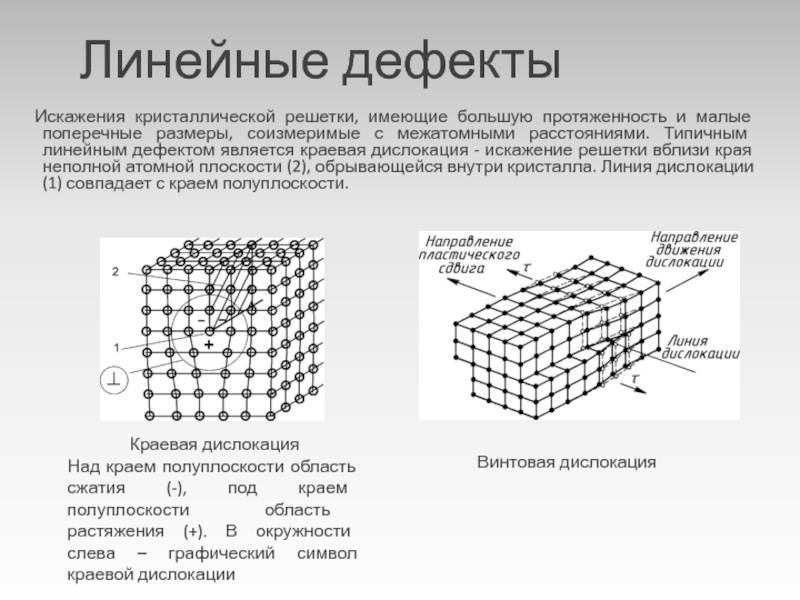
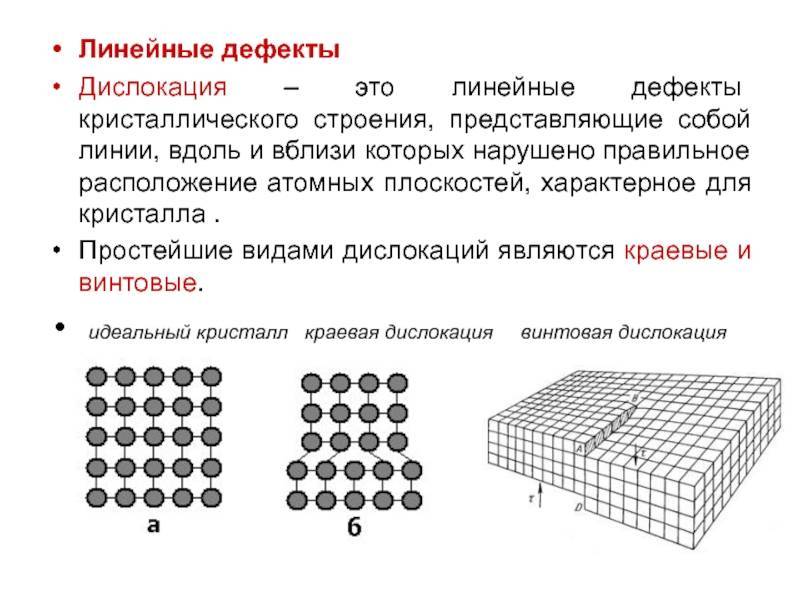
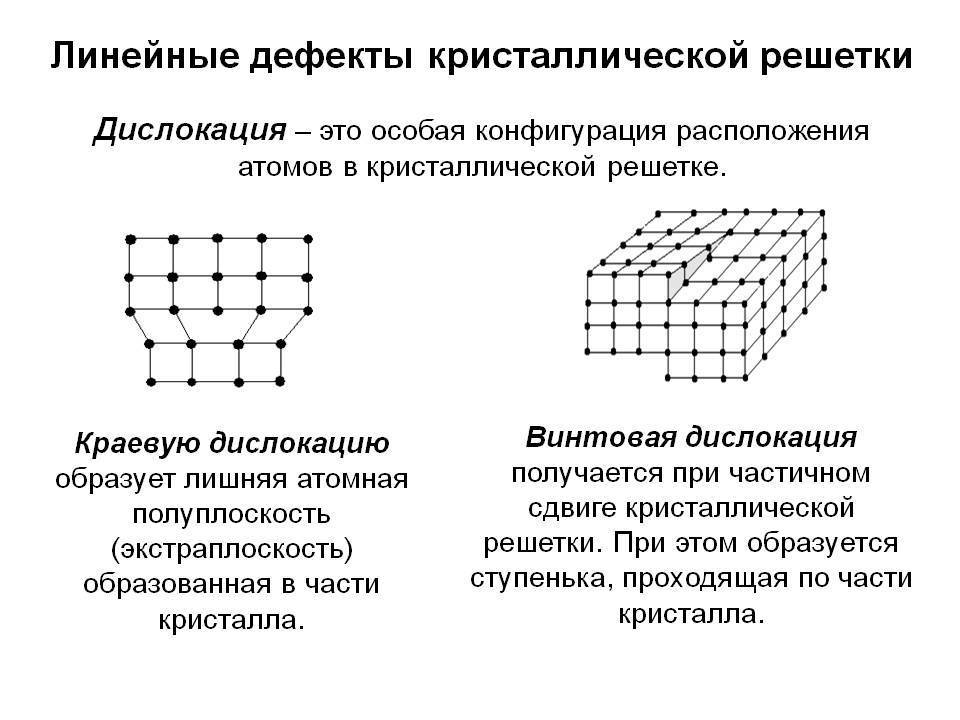
- линейные;
- поверхностные;

Дефекты определяются отсутствием атома или группы атомов в вершинах или гранях кристаллической решетки, смещением этих атомов со своих мест или замещением атома или их группы атомами или молекулами примесей.
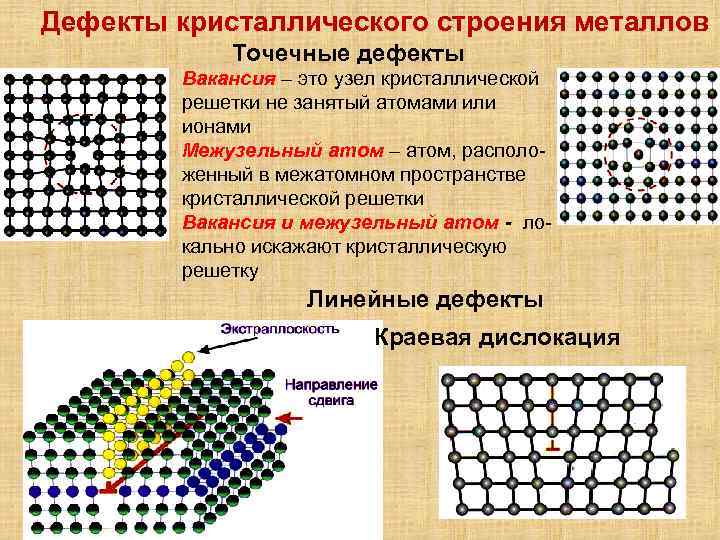
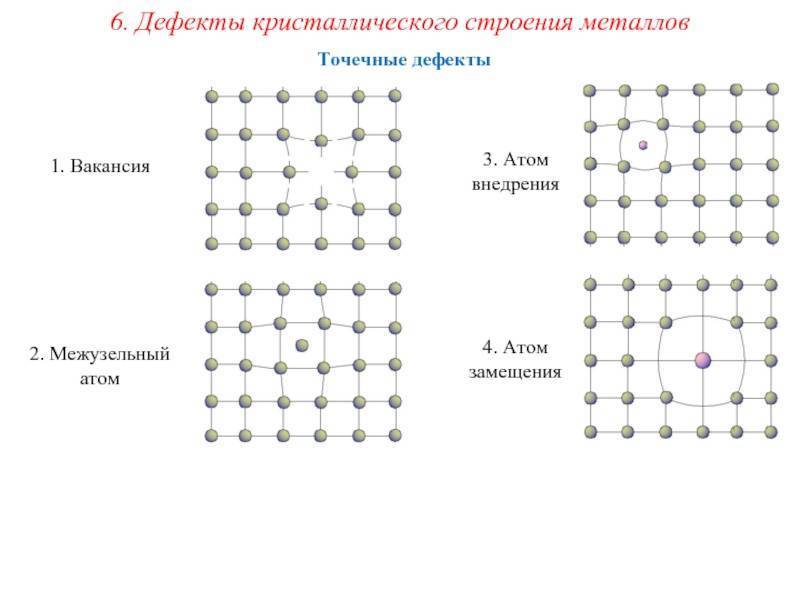
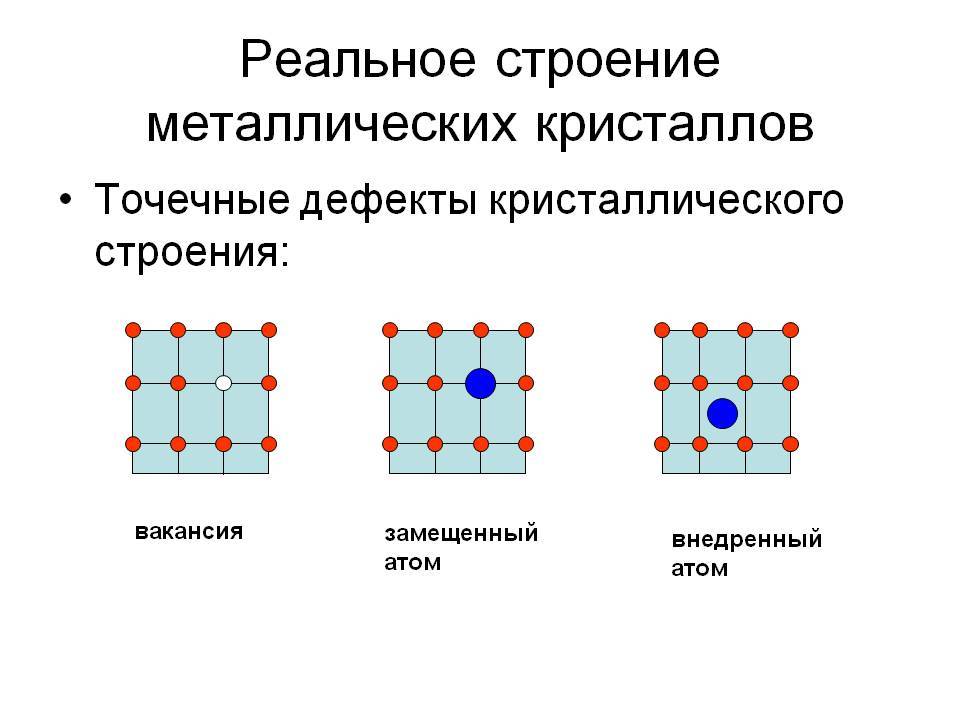
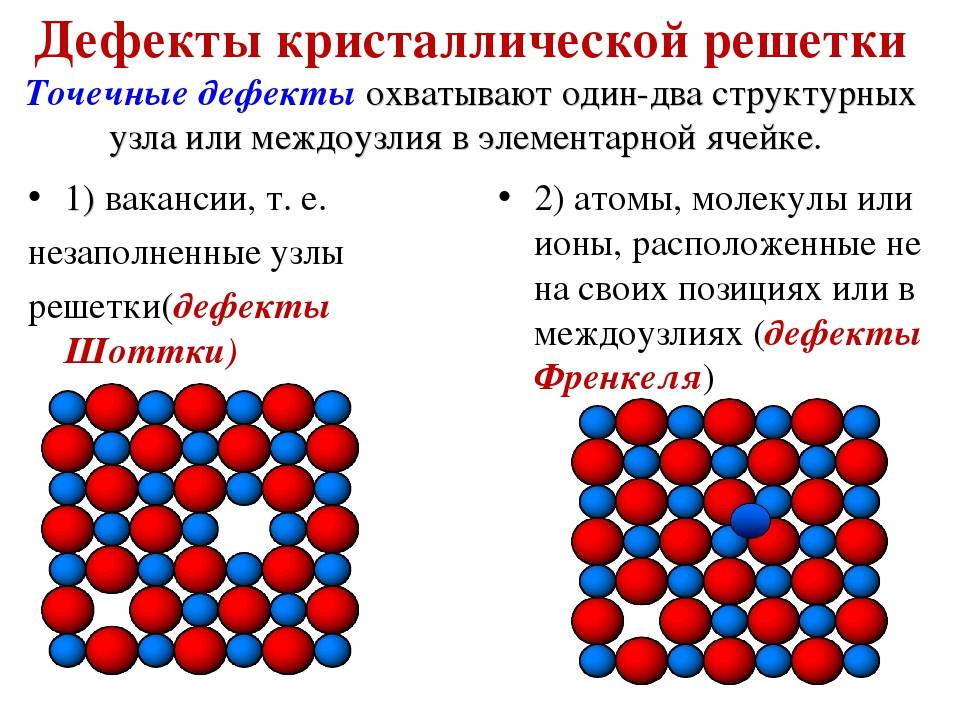
Точечные дефекты (нульмерные)
Точечные дефекты в кристаллах представляют собой искажения решётки с нулевой размерностью, т.е. ни в какой размерности они не обладают структурой решётки.

Типичные точечные несовершенства подразделяются на три группы:
примесные атомы в чистом металле;
вакансии;
межузельные атомы.
Вакансии получают путём нагревания в концентрациях, достаточно высоких для количественных исследований. Для получения аналогичных концентраций межузельных атомов точечные искажения можно получить, выполняя внешнюю работу с кристаллом. Такая работа выполняется в атомном масштабе за счет облучения энергоёмкими частицами. Столкновения между посторонними атомами и атомами решётки вызывают смещения последних от мест замещения к местам внедрения. Таким образом, вакансии и междоузлия производятся в равных количествах. Поскольку одна вакансия и одно междоузлие вместе образуют дефект Френкеля, облучение, по сути, является процессом образования такого дефекта. Это невыгодно по сравнению с экспериментальным исследованием межузельных свойств, поскольку радиационно-индуцированные изменения свойств кристаллов всегда включают роль вакансий.
При пластической деформации также образуются вакансии и межузельные частицы. Хотя деформация обходится намного дешевле, чем облучение частицами, метод не стал общепринятой процедурой для создания точечных дефектов, поскольку не позволяет производить контролируемое образование искажений независимо от сложных сетей дислокаций.
Аномально высокие концентрации точечных несовершенств встречаются в некоторых нестехиометрических интерметаллических соединениях. Здесь вакансии и внедрения уже играют роль дополнительных легирующих элементов и имеют в этом смысле термодинамическое значение.
Другие методы получения точечных дефектов – быстрая закалка, испарение на холодных подложках или лазерный отжиг – зависят от термически активированного производства.
В чистых металлах и в большинстве сплавов вакансии обеспечивают термически активированный перенос атомов и, следовательно, свойства вакансий напрямую влияют на перенос атомов. Свойства вакансии дают информацию о межатомных силах с помощью особых возмущений, которые зависят от вакантного узла решётки.
Молекулярная кристаллическая решетка
Как и в предыдущей группе, в этой находятся вещества с ковалентными связями между атомами. Но физические характеристики этих веществ совершенно иные — они легко плавятся, превращаются в жидкость, растворяются в воде. Почему так происходит? Все дело в том, что здесь кристаллы строятся не из атомов, а из молекул.
Молекулярная кристаллическая решетка — это структура, в узлах которой находятся не атомы, а молекулы.
Внутри молекул атомы имеют прочные ковалентные связи, но сами молекулы связаны между собой слабо. Поэтому кристаллы таких веществ непрочные и легко распадаются.
Молекулярная кристаллическая решетка характерна для воды. При комнатной температуре это жидкость, но стоит нагреть ее до температуры кипения (которая сравнительно низка), как она тут же начинает превращаться в пар, т. е. переходит в газообразное состояние.
Некоторые молекулярные вещества — например, сухой лед CO2, способны преобразоваться в газ сразу из твердого состояния, минуя жидкое (данный процесс называется возгонкой).
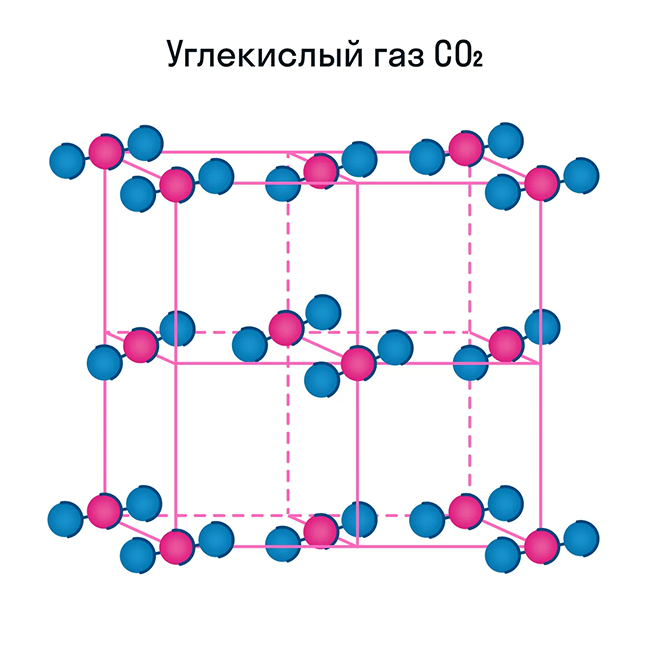
Свойства молекулярных веществ:
небольшая твердость;
низкая прочность;
легкоплавкость;
летучесть;
у некоторых — наличие запаха.
Помимо воды к веществам с молекулярной кристаллической решеткой относятся аммиак NH3, гелий He, радон Rn, йод I, азот N2 и другие. Все благородные газы — молекулярные вещества. Также к этой группе принадлежит и большинство органических соединений (например, сахар).

Черные и цветные металлы
Выше была приведена классификация рассматриваемых элементов в соответствии с их электронным строением и положением в периодической системе. Помимо нее, существует еще одно разделение, которое не связано с атомным строением — это понятие о черных и цветных металлах.
Черным является железо и все сплавы с его участием. Примеры цветных металлов — это алюминий, золото, серебро, медь и другие, а также сплавы, которые не содержат железа. Причина такого разделения проста, черные металлы являются дешевыми и недолговечными (разрушаются в результате коррозии, ржавеют). Наоборот, цветные металлы характеризуются способностью образовывать пленки оксидные, которые предотвращают основную массу материала от дальнейшего химического разрушения.
Почему стоит заказать решетки на окна именно у нас
Компания «Стальной декор» уже 10 лет создает прочные и красивые металлические решетки для окон и устанавливает их в домах и офисах на всей территории Москвы и Московской области. Репутация для нас — это не просто слово. Мы настолько уверены в качестве своих изделий, что назначаем гарантийный срок для каждой металлической конструкции до 5 лет. Отдельное изделие проходит несколько этапов отбраковки, но последнее слово всегда за клиентом!
Если Вы живете на первом этаже или в собственном доме, то наверняка перед Вами периодически возникает вопрос: какие решетки установить на окна? Это необходимый элемент, который позволит Вам защитить свое имущество и защитить в случае необходимости Вашу семью. Именно поэтому, к выбору оконных решеток стоит подходить очень ответственно! Сегодня мы расскажем Вам, как правильно выбрать решетки на окна.
Кроме того, оконные решетки могут украсить и улучшить внешний вид Вашего дома или квартиры. Есть всего два основных вида решеток. Первый — это сварные решетки. В настоящее время ни пользуется популярностью именно этот вид решеток. Их преимущество в прочности и жесткости. Кроме того, цены на такие решетки ниже. Однако сварные решетки не отличаются особо привлекательным дизайном, поэтому не всем покупателям они нравятся.
Кованые решетки привлекают своим внешним видом. Они могут быть очень изящными и стильными. Однако стоимость таких решеток будет гораздо выше, поскольку каждая решетка делается индивидуально под заказ. Если у Вас есть финансы, то кованые решетки будут оптимальным вариантом.
По конструкции решетки бывают:
* из прутка с круглым или квадратным сечением (они наиболее крепкие, благодаря своей толщине от 12 до 20 мм);
* из полосы с прямоугольным сечением (этот профиль обойдется вам дешевле, однако будет отличаться меньшей надежностью).
Если Вы решили делать решетки на заказ, обратите внимание на материал
, из которого они будут изготовлены. Вы вполне можете заказать себе решетки на окна, изготовленные из сочетания двух конструкций. По типу монтажа решетки на окна мало чем различаются
Мастер лишь выбирает способ крепления, который зависит от особенностей изделия. Решетки могут быть стационарными, распашными, раздвижными или съемными. Все что Вам необходимо — это решить, какой вид решеток необходим в Вашем случае
По типу монтажа решетки на окна мало чем различаются. Мастер лишь выбирает способ крепления, который зависит от особенностей изделия. Решетки могут быть стационарными, распашными, раздвижными или съемными. Все что Вам необходимо — это решить, какой вид решеток необходим в Вашем случае.
Стационарные решетки крепятся раз и навсегда. Вы не сможете их открыть, и их конструкция максимально надежна. Процесс крепления:
* В торцах оконного проема нужно просверлить отверстия под крепления решетки. В зависимости от размеров креплений, диаметр отверстий может варьироваться от 12 до 20 мм.
* После этого решетка крепится ко всем четырем сторонам оконного проема с помощью специальных крюков-штырей, прижимающих металлическое изделие к стенам.
Распашные металлические решетки позволят Вам периодически их раскрывать, как створки. По желанию, Вы можете заказать решетки с одной или двумя подвижными створками. Процесс крепления такой же, какой был описан выше. Однако крепление решетки происходит только в боковых сторонах оконного проема.
Раздвижные решетки
имеют систему, похожую на систему раздвижного механизма
Процесс крепления:
* При монтаже нужно прикрепить полозы (направляющие шины решетки) к торцам оконного проема для свободного хода конструкции во время раздвигания, а после вставить решетку в созданную раму.
* Обратите внимание, что у раздвижных решеток есть свои недостатки: конструкция из склепанной крест-накрест полосы снижает защитные свойства и жесткость
И, наконец, съемные решетки монтируются в межоконный проем. Монтировать их можно как с помощью крюков, так и с использованием ввинчиваемых болтов.
Металлическая кристаллическая решётка
Из-за наличия в узлах ионов, может показаться, что металлическая решетка похожа на ионную. На самом деле, это две совершенно разные модели, с разными свойствами.
Металлическая гораздо гибче и пластичнее ионной, для неё характерна прочность, высокая электро- и теплопроводность, эти вещества хорошо плавятся и отлично проводят электрический ток. Это объясняется тем, что в узлах находятся положительно заряженные ионы металлов (катионы), которые могут перемещаться по всей структуре, тем самым обеспечивают течение электронов. Частицы хаотично движутся около своего узла (они не имеют достаточной энергии, чтобы выйти за пределы), но как только появляется электрическое поле, электроны образуют поток и устремляются из положительной в отрицательную область.
Металлическая кристаллическая решётка характерна для металлов, например: свинец, натрий, калий, кальций, серебро, железо, цинк, платина и так далее. Помимо прочего, она подразделяется ещё на несколько типов упаковок: гексагональная, объёмно центрированная (наименее плотная) и гранецентрированная. Первая упаковка характерна для цинка, кобальта, магния, вторая для бария, железа, натрия, третья для меди, алюминия и кальция.
Таким образом, от типа решётки зависят многие свойства, а также строение вещества. Зная тип, можно предсказать, к примеру, какой будет тугоплавкость или прочность объекта.
Кованая решетка плюсы и минусы
У кованой решетки есть один неоспоримый плюс — это ее уникальность. Кованые изделия всегда неординарны и оригинальны. Они похожи на изысканное воздушное кружево. Причем, если из огромного ассортимента типовых кованых решеток, вам ничего не понравится, то вы можете сами поучаствовать в творческом процессе. Мастер легко создаст решетку по вашему эскизу.
К минусам кованой решетки можно отнести ее стоимость. В среднем цена изделия начинается с 2000 рублей, что в два раза больше стоимости сварной решетки. Для многих покупателей такой разброс цен — это важный фактор. Также понятно, что из-за сложности конструкции произвести необходимые расчеты по прочности не представляется возможным. Однако это компенсируется большим количеством соединительных точек в изделии и достаточно плотным заполнением пространства решетки гнутыми металлическими формами.
Геохимия железа
Гидротермальный источник с железистой водой. Окислы железа окрашивают воду в бурый цвет Железо — один из самых распространённых элементов в Солнечной системе, особенно на планетах земной группы, в частности, на Земле. Значительная часть железа планет земной группы находится в ядрах планет, где его содержание, по оценкам, около 90 %. Содержание железа в земной коре составляет 5 %, а в мантии около 12 %. Из металлов железо уступает по распространённости в коре только алюминию. При этом в ядре находится около 86 % всего железа, а в мантии 14 %.
Геохимические свойства железа
Важнейшая геохимическая особенность железа — наличие у него нескольких степеней окисления. Железо в нейтральной форме — металлическое — слагает ядро земли, возможно, присутствует в мантии и очень редко встречается в земной коре. Закисное железо FeO — основная форма нахождения железа в мантии и земной коре. Окисное железо Fe2O3 характерно для самых верхних, наиболее окисленных, частей земной коры, в частности, осадочных пород.
По кристаллохимическим свойствам ион Fe2+ близок к ионам Mg2+ и Ca2+ — другим главным элементам, составляющим значительную часть всех земных пород. В силу кристаллохимического сходства железо замещает магний и, частично, кальций во многих силикатах. При этом содержание железа в минералах переменного состава обычно увеличивается с уменьшением температуры.
Минералы железа
В земной коре железо распространено достаточно широко — на его долю приходится около 4,1 % массы земной коры (4-е место среди всех элементов, 2-е среди металлов). В мантии и земной коре железо сосредоточено главным образом в силикатах, при этом его содержание значительно в основных и ультраосновных породах, и мало — в кислых и средних породах.
Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк (гематит, Fe2O3; содержит до 70 % Fe), магнитный железняк (магнетит, FeFe2O4, Fe3O4; содержит 72,4 % Fe), бурый железняк или лимонит (гётит и гидрогётит, соответственно FeOOH и FeOOH·nH2O), а также шпатовый железняк (сидерит, карбонат железа(II), FeCO3; содержит около 48 % Fe). Гётит и гидрогётит чаще всего встречаются в корах выветривания, образуя так называемые «железные шляпы», мощность которых достигает несколько сотен метров. Также они могут иметь осадочное происхождение, выпадая из коллоидных растворов в озёрах или прибрежных зонах морей. При этом образуются оолитовые, или бобовые, железные руды. В них часто встречается вивианит Fe(3PO4)2·8H2O, образующий чёрные удлинённые кристаллы и радиально-лучистые агрегаты.
В природе также широко распространены сульфиды железа — пирит FeS2 (серный или железный колчедан) и пирротин. Они не являются железной рудой — пирит используют для получения серной кислоты, а пирротин часто содержит никель и кобальт.
По запасам железных руд Россия занимает первое место в мире. Содержание железа в морской воде — 1×10−5—1×10−8 %.
Особенности строения кристаллической решетки металлов металлический блеск
Найдите по таблице два металла с объемно-центрированной и гранецентрированной упаковкой с близкими температурами плавления (максимальное отличие 20 градусов). Посчитайте отношение их коэффициентов линейного расширения. Значение запишите с точностью до второго знака после запятой.
Прочитайте текст и выполните задания 16—18.
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет кристаллическое строение металлов. К специфическим свойствам рассматриваемых веществ относят следующие:
1. Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым серебристо-белым цветом. Лишь некоторые (золото, медь, сплавы) отличаются.
2. Ковкость и пластичность — способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
3. Электропроводность и теплопроводность — одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя. Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.
Связь между коэффициентами линейного расширения,
температурами плавления металлов и симметрией
Кристалл — это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится изображение в виде правильного геометрического тела какой-либо формы. Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку. Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки.
Сама элементарная ячейка – это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства. Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность – в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
Реальный кристалл металла
Какой бы химический металлический элемент не рассматривался, в действительности он представляет собой твердое вещество, в котором маленькие монокристаллы (зерна) соединены друг с другом в различных ориентациях. Такая структура образует поликристалл. В нем, помимо границ зерен, присутствуют дефекты всех четырех типов, включая примеси таких неметаллов, как кислород, азот и водород. Последний из-за своих размеров легко проникает в любую кристаллическую решетку, образует с ее ионами твердые фазы, которые приводят к охрупчиванию металла, что является одной из актуальных проблем металловедения.
Какие металлы бывают?
Металлы в периодической системе Менделеева делятся на несколько групп. Перечислим и кратко охарактеризуем их:
- Щелочные. Эти металлы имеют всего 1 валентный электрон, они чрезвычайно химически активны, имеют низкую плотность и являются отличными проводниками тепла и электричества. Примерами их являются литий, натрий и калий.
- Щелочноземельные. К ним относятся кальций, магний, стронций. Эти металлы имеют 2 валентных электрона, поэтому они также являются химически активными.
- Переходные. Это металлы с переменной валентностью, которые имеют пустые или полупустые орбитали d и f типа. Это самая многочисленная группа металлов. К ним относятся титан, ванадий, хром, никель, вольфрам, осмий, золото и многие другие.
- Лантаноиды и актиноиды. Большая часть этих элементов является нестабильными и проявляет различную степень радиоактивности.
- Постпереходные. Это те элементы, после которых по периоду идут металлоиды, а затем неметаллы. Самыми известными из них являются свинец, алюминий и олово.