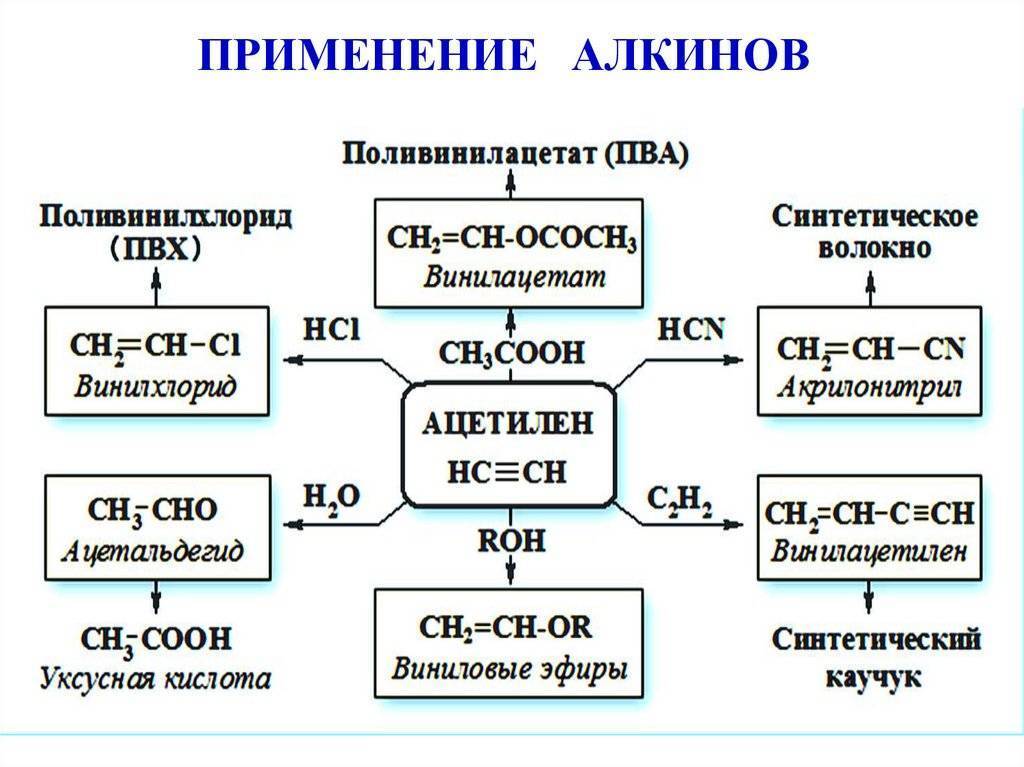
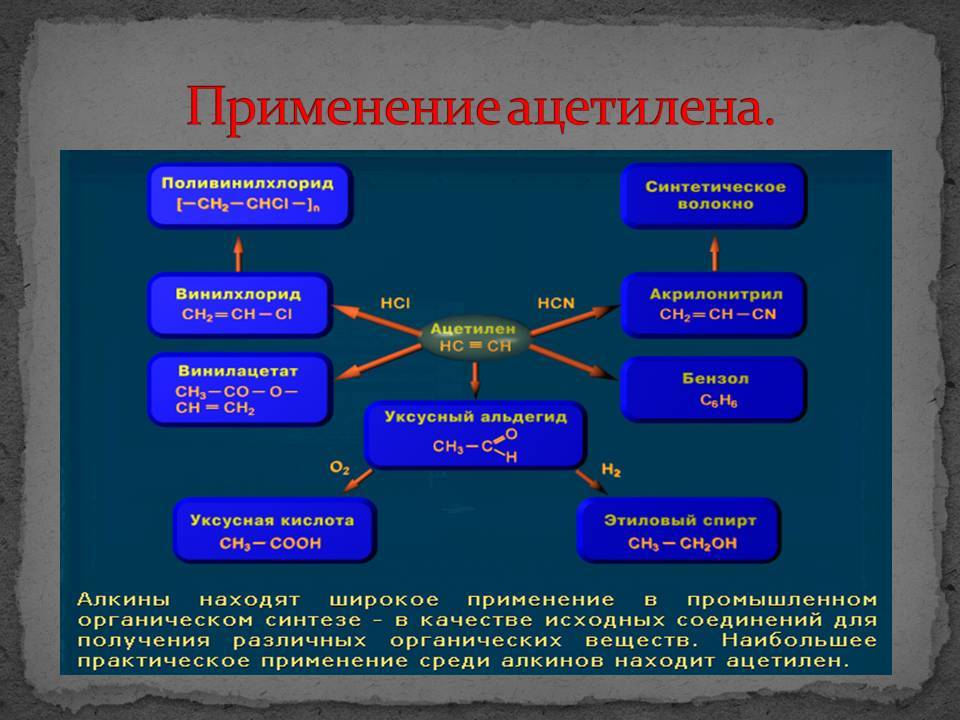
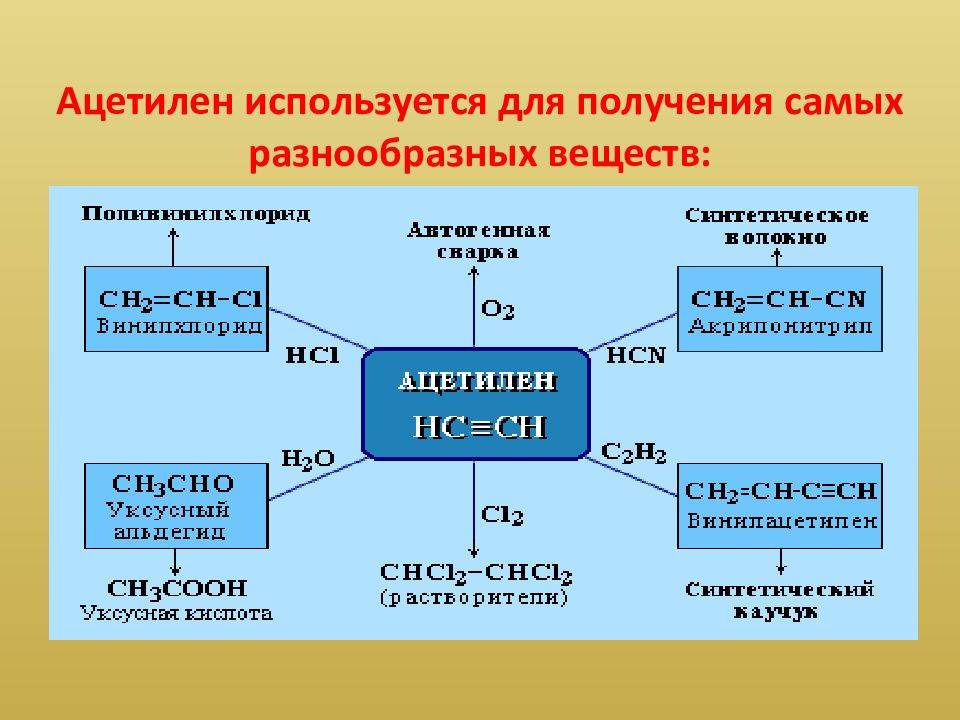
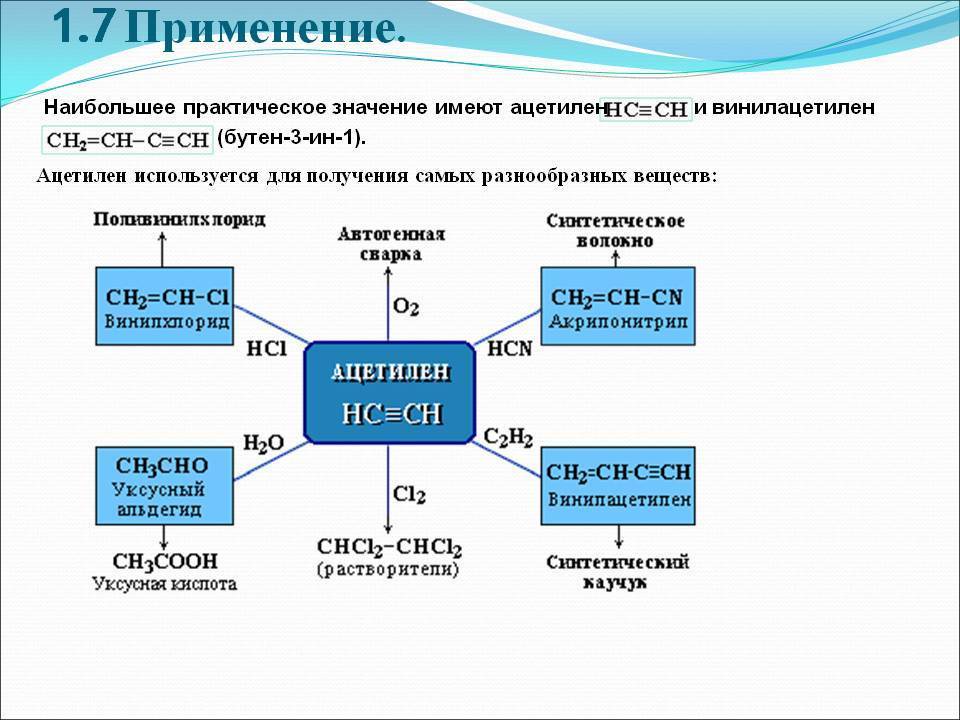
Применение ацетилена при сварке
Ацетилен – основной горючий газ, используемый при газовой сварке, а также широко применяется для газовой резки (кислородной резки). Температура ацетилено-кислородного пламени может достигать 3300°C. Благодаря этому ацетилен по сравнению с более доступными горючими газами (пропан-бутаном, природным газом и др.) обеспечивает более высокое качество и производительность сварки.
Снабжение постов ацетиленом для газовой сварки и резки может осуществляться
- от баллонов с ацетиленом и
- от ацетиленового генератора.
Для хранения ацетилена обычно используются стандартные баллоны емкостью 40 л, окрашенные в белый цвет, с надписью «Ацетилен» красного цвета (ПБ 10-115-96, ГОСТ 949-73). Согласно ГОСТ 5457-75 для газопламенной обработки металлов применяется технический ацетилен растворенный марки Б и газообразный.
Таблица. Характеристики марок технического ацетилена (ГОСТ 5457-75), используемого при сварке и резке.
| Параметр | Ацетилен технический | ||
| растворенный марки Б | газообразный | ||
| первого сорта | второго сорта | ||
| Объемная доля ацетилена C2H2, %, не менее | 99,1 | 98,8 | 98,5 |
| Объемная доля воздуха и других газов, малорастворимых в воде, %, не более | 0,8 | 1,0 | 1,4 |
| Объемная доля фосфористого водорода PH3, %, не более | 0,02 | 0,05 | 0,08 |
| Объемная доля сероводорода H2S, %, не более | 0,005 | 0,05 | 0,05 |
| Массовая концентрация водяных паров при давлении 101,3 кПа (760 мм рт. ст.) и температуре 20°С, г/м3, не более | 0,5 | 0,6 | не нормируется |
| что соответствует температуре насыщения, не выше (°C) | -24 | -22 |
Баллоны заполнены пористой массой, пропитанной ацетоном. Ацетилен хорошо растворяется а ацетоне: при нормальной температуре и давлении в 1 л ацетона растворяется 23 л ацетилена (в 1 л бензина растворяется 5,7 л ацетилена, в 1 л воды – 1,15 л ацетилена). Пористая масса выполняет следующие функции:
- повышает безопасность при работе с баллоном – за счет пористой массы общий объем ацетилена разделен на отдельные ячейки; таким образом, вероятность распространения общего фронта горения и взрыва значительно уменьшается;
- позволяет повысить количество ацетилена в баллоне, ускорить процесс его растворения при заполнении баллона и выделении при отборе газа – поскольку при использовании пористой массы, пропитанной ацетоном, обеспечивается большая поверхность взаимного контакта между газом и ацетоном.
В качестве пористых масс могут применяться активированный уголь, пемза, волокнистый асбест.
Таблица. Допустимое давление газа в баллоне в зависимости от температуры (при номинальном давлении 1,9 МПа / +20°С) (ГОСТ 5457-75)
| Температура, °С | -5 | +5 | +10 | +15 | +20 | +25 | +30 | +35 | +40 | ||
| Давление в баллоне, не более | МПа | 1,34 | 1,4 | 1,5 | 1,65 | 1,8 | 1,9 | 2,15 | 2,35 | 2,6 | 3 |
| кгс/см2 | 13,4 | 14 | 15 | 16,5 | 18 | 19 | 21,5 | 23,5 | 26 | 30 |
Таблица. Остаточное давление газа в баллоне, поступающем от потребителя (ГОСТ 5457-75)
| Температура, °С | до 0 | от 0 до +15 | от +15 до +25 | от +25 до +35 | |
| Остаточное давление в баллоне, не менее | МПа | 0,05 | 0,1 | 0,2 | 0,3 |
| кгс/см2 | 0,5 | 1 | 2 | 3 |
40-литровые баллоны с максимальным давлением газа 1,9 МПа при температуре 20°С обычно заполняют 5–5,8 кг ацетилена (4,6–5,3 м3 газа при температуре 20°С и давлении 760 мм рт. ст.). Масса ацетилена в баллоне определяется по разности масс баллона до и после наполнения газом. Объем ацетилена равен отношению его массы и плотности. Так, объем 5,5 кг ацетилена при температуре 20°С и давлении 760 мм рт. ст. составляет 5,5/1,09 = 5,05 м3.
Таблица. Сравнительные характеристики ацетилена, пропана и метилацетилен-алленовой фракции (МАФ)
| Параметр | ацетилен | пропан | МАФ |
| Чувствительность к удару, безопасность | нестабилен | стабилен | стабилен |
| Токсичность | незначительная | ||
| Предел взрываемости в воздухе (%) | 2,2–81 | 2,0–9,5 | 3,4–10,8 |
| Предел взрываемости в кислороде (%) | 2,3–93 | 2,4–57 | 2,5–60 |
| Температура пламени (°С) | 3087 | 2526 | 2927 * |
| Реакции с обычными металлами | избегать сплавов, содержащих более 70% меди | незначительные ограничения | избегать сплавов, содержащих более 65–67% меди |
| Склонность к обратному удару | значительная | незначительная | незначительная |
| Скорость сгорания в кислороде (м/с) | 6,10 | 3,72 | 4,70 |
| Плотность газа (кг/м3) | 1,17 (при 0°С) 1,09 (при 20°С) | 2,02 (при 0°С) | 1,70 (при 0°С) * |
| Плотность в жидком состоянии при 15,6°С (кг/м3) | – | 513 | 575 |
| Отношение расхода кислорода к горючему газу (м3/м3) при нормальном пламени | 1–1,2 | 3,50 | 2,3–2,5 |
Это интересно: Балластный реостат РБ-302,РБ-306 — технические характеристики, схемы
Технология и режимы сварки
Ацетилено — кислородные смеси применяют для соединения деталей из углеродистых и низколегированных сталей. Например, этот метод широко применяют для создания неразъемных соединений трубопроводов. Например, труб диаметром 159 мм с толщиной стенок не более 8 мм. Но существуют и некоторые ограничения, так соединение таким методом сталей марок 12×2M1, 12×2МФСР недопустимо.

Сварка при помощи ацетилена

Пламя при ацетиленовой сварке
Выбор параметров режима
Для приготовления смеси необходимой для соединения металлов используют формулу 1/1,2. При обработке заготовок из легированных сталей сварщик должен отслеживать состояние пламени. В частности, нельзя допускать переизбытка ацетилена.
Расход смеси с формулой кислород/ацетилен составляет 100-130 дм3/час на 1 мм толщины. Мощность пламени регулируют с помощью горелки, которые подбирают в зависимости от используемого материала, его характеристик, толщины и пр
Для выполнения сварки при помощи ацетилена применяют сварочную проволоку. Ее марка должна соответствовать марке сталей свариваемых деталей. Диаметр проволоки определяют в зависимости от толщины свариваемого металла.
Для удобства технологов и непосредственно сварщиков существует множество таблиц, на основании которых можно довольно легко выбрать сварочный режим. Для этого необходимо знать следующие параметры:
- толщину стенки свариваемых заготовок;
- вид сварки — левый, правый;
На основании этого можно определить диаметр присадочной проволоки и подобрать расход ацетилена. К примеру, толщина составляет 5-6 мм, для выполнения работ будет использован наконечник № 4. То есть на основании табличных данных диаметр проволоки будет составлять для левой сварки 3,5 мм, для правой 3. Расход ацетилена в таком случае будет составлять при левом способе 60 -780 дм3/час, при правом 650-750 дм3/час.
Сварку выполняют небольшими участками по 10-15 мм. Работа производится в следующей последовательности. На первом этапе выполняют оплавление кромок. После этого выполняют наложение корня шва. По окончании формирования корня, можно продолжать сварку далее. Если толщина заготовок составляет 4 мм то сварку допустимо выполнять в один слой. Если толщина превышает указанную, то необходимо наложить второй. Его укладывают только после того, как выполнен корень шва по всей заданной длине.
Для улучшения качества сварки допускается выполнение предварительного нагрева. То есть будущий сварной стык прогревают с помощью горелки. Если принят за основу такой способ, то прогрев надо выполнять после каждой остановки заново.
Выполнение швов газом может выполняться в любом пространственном положении. Например, при выполнении вертикального шва существуют свои особенности. Так, вертикальный шов должен исполняться снизу вверх.
При выполнении сварочных работ перерывы в работе недопустимы, по крайней мере до окончания всей разделки шва. При остановке в работе горелку необходимо отводить медленно, в противном случае, могут возникнуть дефекты шва — раковины и поры. Интересная особенность существует при сварке трубопроводов, в ней не допустим сквозняк и поэтому концы труб необходимо заглушать.
Преимущества
Упоминание о газовой сварке моментально наводит на мысли об ацетилене. Действительно для этого процесса чаще всего применяют этот газ. Он в сочетании с кислородом обеспечивает самую высокую температуру горения пламени. Но в последние годы из-за развития различных видов сварки использование этого вида соединения металлов несколько снизилось. Более того, в некоторых отраслях произошел полный отказ от применения этих технологий. Но для выполнения определенного вида ремонтных работ она до сих пор остается незаменима. Применение ацетилена позволяет получить следующие преимущества:
- максимальная температура пламени;
- существует возможность генерации ацетилена непосредственно на рабочем месте или приобретения его в специальных емкостях;
- довольно низкая стоимость, в сравнении с другими горючими газами.
Вместе с тем, у ацетилена есть и определенные недостатки, которые ограничивают его использование. Самый главный – это взрывоопасность. При работе с этим газом необходимо строго соблюдать меры безопасности. В частности, работы должны выполняться в хорошо проветриваемом помещении. При нарушении режимов работы возможно появление некоторых дефектов, например, пережогов.
Преимущества
Газ является непредельным углеводородом, который обладает тройной связью атомов углерода. Формула ацетилена – С2Н2. При этом структурная формула ацетилена выглядит следующим образом Н-С=С-Н, так как связь идет между атомами углерода.
Химические и физические свойства
В нормальных условиях газ является бесцветным. Он легче воздуха. В техническом ацетилене имеются добавки, которые придают ему резкий запах, но в чистом виде он ни чем не пахнет. Лучше всего газ растворяется в ацетоне, но в воде он мало растворим. Температура кипения достигает -83,6 градусов Цельсия.
Газ требует очень аккуратного обращения. Баллон может взорваться от обыкновенного удара при падении или при нагреве около 500 градусов Цельсия. Воспламениться струя может даже от статического электричества от пальца человеческой руки. Молярная масса ацетилена составляет 26 г/моль. Температура горения ацетилена в ядре пламени может составлять более 2600 градусов Цельсия.
Химические свойства ацетилена показывают, в какие реакции может вступать субстанция с другими веществами. В присутствии катализаторов, в частности солей ртути, газ образует уксусный альдегид. Благодаря наличию тройной связи, молекулы вещества имеют большой запас энергии. Это обеспечивает ей высокую теплоту сгорания, которая составляет 14 000 ккал/м3. Если при сгорании добавить струю кислорода, то температура пламени достигнет более 3100 градусов Цельсия. Газ может полимеризироваться в такое вещество как бензол и прочие органические соединения, к примеру, винилацетилен или полиацетилен. Полимеризация в бензол происходит при температуре в 500 градусов Цельсия и при наличии графита. Если в качестве катализатора использоваться трикарбонил никеля, то данная реакция может пройти при температуре в 65 градусов Целься. Ацетилен обладает очень сильными кислотными свойствами. Атомы водорода могут легко отщепиться в качестве протонов. В эфирном растворе металмагнийбромида данный газ вытесняет метан. В сочетании с солями одновалентной меди и серебра ацетилен образует взрывчатый нерастворимый осадок.
Состав
Горение ацетилена и прочие его практические свойства во многом зависят от состава. Даже небольшие отклонения от нормы могут привести к тому, что газ поменяет свои характеристики. Поэтому, выделяют несколько основных сортов, отличающихся друг от друга по своему составу.
Состав ацетилена газообразного технического:
- Основной газ – 98,5%;
- Воздух – 1,4%;
- Фосфорный водород – 0,08%;
- Сероводород – 0,05%.
Растворенное вещество первого сорта марки Б должно обладать следующим составом:
- Основной газ – 99,1%;
- Воздух – 0,8%;
- Фосфорный водород – 0,02%;
- Сероводород – 0,005%.
Растворенное вещество второго сорта марки Б должно обладать следующим составом:
- Основной газ – 98,8%;
- Воздух – 1%;
- Фосфорный водород – 0,05%;
- Сероводород – 0,05%.
Растворенное вещество марки А должно обладать следующим составом:
- Основной газ – 99,5%;
- Воздух – 0,5%;
- Фосфорный водород – 0,005%;
- Сероводород – 0,002%.
Технология и режимы сварки
Перед началом сварки нужно подобрать баллон с ацетиленом и понять саму его конструкцию.

Конструкция баллона с ацетиленом
Потом подбирается горелка требуемого размера от 0 до 5. Толщина этого инструмента определяет расход газа, а также ширину образуемого шва. Чтобы проверить готовность изделия к работе, ее нужно продуть ацетиленом до тех пор, чтобы почувствовать его запах.
Поджог газа осуществляется еще до добавления кислорода. После загорания можно добавить понемногу струю кислорода, пока не образуется устойчивое пламя. Выходное давление основного газа должно быть до 4 атмосфер, а дополнительного – до 2 атмосфер. Затем подбирается мощность пламени согласно толщине свариваемого металла.
Заранее очищенные заготовки предварительно прогреваются пламенем горелки до нужной температуры. После этого добавляется сварочная проволока, которая вместе с основным металлом образует сварочную ванну. Процесс сварки может проводиться как правым, так и левым способом. После окончания процедуры горение ацетилена поможет постепенному охлаждению шва с подогревом.
Заключение
Разбираясь, для чего нужен ацетилен в сварочной области, в первую очередь нужно думать о безопасности. Отличные практические качества и низкая стоимость газа не позволяют отказаться от него полностью из-за взрывоопасности. Любой специалист может оценить все преимущества работы с ним, но сложности хранения затрудняют его применение в домашних условиях.
Виды ацетилена
Промышленность выпускает два вида ацетилена — твердый и в виде газа.
Газообразный
Ацетилен обладает резким запахом и это дает определённые преимущества при его утечке. По своей массе он близок к атмосферному воздуху.
Жидкий
Жидкий ацетилен не обладает ни каким цветом. У него есть одна особенность он преломляет цвет. Ацетилен и жидкий, и газообразный, представляет собой опасное вещество. То есть при нарушении правил обращения с ним взрыв может произойти в любую секунду, даже при комнатной температуре. Для повышения безопасности при обращении с ним, применяют так называемую флегматизацией. То есть в ёмкости, предназначенной для хранения ацетилена размещают пористое вещество. Которое снижает его опасность
Реакции присоединения
Тройная связь состоит из σ-связи и двух π-связей. Сравним характеристики одинарной связи С–С, тройной связи С≡С и связи С–Н:
| Энергия связи, кДж/моль | Длина связи, нм | |
| С–С | 348 | 0,154 |
| С≡С | 814 | 0,120 |
| С–Н | 435 | 0,107 |
Таким образом, тройная связь С≡С короче, чем одинарная связь С–С, поэтому π-электроны тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью и подвижностью. Реакции присоединения по тройной связи к алкинам протекают сложнее, чем реакции присоединения по двойной связи к алкенам.
Для алкинов характерны реакции присоединения по тройной связи С≡С с разрывом π-связей.
1.1. Гидрирование
Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов.
Например, при гидрировании бутина-2 в присутствии никеля образуется сначала бутен-2, а затем бутан.
При использовании менее активного катализатора (Pd, СaCO3, Pb(CH3COO)2) гидрирование останавливается на этапе образования алкенов.
Например, при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.
1.2. Галогенирование алкинов
Присоединение галогенов к алкинам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
При взаимодействии с алкинами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на тройную связь.
Например, при бромировании пропина сначала образуется 1,2-дибромпропен, а затем — 1,1,2,2-тетрабромпропан.
Аналогично алкины реагируют с хлором, но обесцвечивания хлорной воды при этом не происходит, потому что хлорная вода и так бесцветная)
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкинов
Алкины присоединяют галогеноводороды. Реакция протекает по механизму электрофильного присоединения с образованием галогенопроизводного алкена или дигалогеналкана.
Например, при взаимодействии ацетилена с хлороводородом образуется хлорэтен, а затем 1,1-дихлорэтан.
При присоединении галогеноводородов и других полярных молекул к симметричным алкинам образуется, как правило, один продукт реакции, где оба галогена находятся у одного атома С.
Окисление алкинов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
2.1. Горение алкинов
Алкины, как и прочие углеводороды, горят с образованием углекислого газа и воды.
Уравнение сгорания алкинов в общем виде:
CnH2n-2 + (3n-1)/2O2 → nCO2 + (n-1)H2O + Q
| Например, уравнение сгорания пропина: |
C3H4 + 4O2 → 3CO2 + 2H2O
2.2. Окисление алкинов сильными окислителями
Алкины реагируют с сильными окислителями (перманганаты или соединения хрома (VI)). При этом происходит окисление тройной связи С≡С и связей С-Н у атомов углерода при тройной связи. При этом образуются связи с кислородом.
При окислении трех связей у атома углерода в кислой среде образуется карбоксильная группа СООН, четырех — углекислый газ СО2. В нейтральной среде — соль карбоновой кислоты и карбонат (гидрокарбонат) соответственно.
Таблица соответствия окисляемого фрагмента молекулы и продукта:
| Окисляемый фрагмент | KMnO4, кислая среда | KMnO4, H2O, t |
| R-C≡ | R-COOH | -COOMe |
| CH≡ | CO2 | Me2CO3 (MeHCO3) |
При окислении бутина-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента СН3–C≡, поэтому образуется уксусная кислота:
При окислении 3-метилпентина-1 перманганатом калия в серной кислоте окислению подвергаются фрагменты R–C и H–C , поэтому образуются карбоновая кислота и углекислый газ:
При окислении алкинов сильными окислителями в нейтральной среде углеродсодержащие продукты реакции жесткого окисления (кислота, углекислый газ) могут реагировать с образующейся в растворе щелочью в соотношении, которое определяется электронным балансом с образованием соответствующих солей.
| Например, при окислении бутина-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента R–C≡, поэтому образуется соль уксусной кислоты – ацетат калия |
Аналогичные органические продукты образуются при взаимодействии алкинов с хроматами или дихроматами.
Окисление ацетилена протекает немного иначе, σ-связь С–С не разрывается, поэтому в кислой среде образуется щавелевая кислота:
В нейтральной среде образуется соль щавелевой кислоты – оксалат калия:
Обесцвечивание раствора перманганата калия — качественная реакция на тройную связь.
Взрывоопасность ацетилена и безопасность при обращении с ним:
Ацетилен обладает взрывоопасными свойствами.
Поэтому обращение с ацетиленом требует строгого соблюдения правил техники безопасности.
Ацетилен горит и взрывается даже в отсутствии кислорода и других окислителей.
Смеси ацетилена с воздухом взрывоопасны в очень широком диапазоне концентраций.
Струя ацетилена, выпущенная на открытый воздух, может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки.
Взрываемость ацетилена зависит от множества факторов: давления, температуры, чистоты ацетилена, содержания в нем влаги, наличия катализаторов и пр. веществ и ряда других причин.
Температура самовоспламенения ацетилена при нормальном – атмосферном давлении колеблется в пределах 500-600 °C. При повышении давления существенно уменьшается температура самовоспламенения ацетилена. Так, при давлении 2 кгс/см2 (0,2 МПа, 1,935682 атм.) температура самовоспламенения ацетилена равна 630 °C. А при давлении 22 кгс/см2 (2,2 МПа, 21,292502 атм.) температура самовоспламенения ацетилена равна 350 °С.
Присутствие в ацетилене частиц различных веществ увеличивают поверхность его контакта и тем самым снижает температуру самовоспламенения при атмосферном давлении. Например, активированный уголь снижает температуру самовоспламенения ацетилена до 400 °С, гидрат оксида железа (ржавчина) – до 280-300 °С, железная стружка – до 520 °С, латунная стружка – до 500-520 °С, карбид кальция – до 500 °С, оксид алюминия – до 490 °С, медная стружка – 460 °С, оксид железа – 280 °С, оксид меди – до 250 °С.
Взрывоопасность ацетилена уменьшается при разбавлении ацетилена другими газами, например азотом, метаном или пропаном.
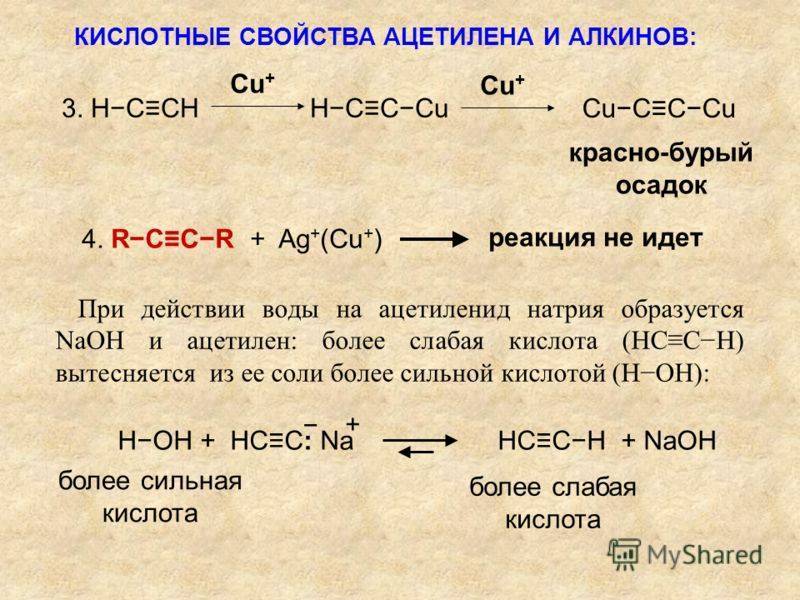
При определенных условиях ацетилен реагирует с медью, серебром и ртутью образуя взрывоопасные соединения. Поэтому при изготовлении ацетиленового оборудования (например, вентилей баллонов) запрещается применять сплавы, содержащие более 70 % Cu.
Для хранения и перевозки ацетилена используются специальные стальные баллоны белого цвета (с красной надписью «А»), заполненные инертным пористым материалом (например, древесным углём). При этом ацетилен хранится и перевозится в указанных баллонах в виде раствора ацетилена в ацетоне под давлением 1,5-2,5 МПа.
карта сайта
как получить ацетилен реакция ацетилен этен 1 2 вещество кислород водород связь является углекислый газ бромная вода уравнение реакции масса объем полное сгорание моль молекула смесь превращение горение получение ацетилена напишите уравнение реакций ацетилен
comments powered by HyperComments
Опыт 1. Получение ацетилена и его горение.
⇐ ПредыдущаяСтр 5 из 8Следующая ⇒
Реактивы и материалы: карбид кальция СаС2 (в кусочках). Оборудование: газоотводная трубка с оттянутым концом.
Работу с ацетиленом необходимо проводить в вытяжном шкафу, так как неочищенный ацетилен, полученный из карбида кальция, содержит вредные, неприятно пахнущие примеси.
В пробирку помещают маленький кусочек карбида кальция СаС2, добавляют 2 капли воды и закрывают пробирку пробкой с газоотводной трубкой, имеющей оттянутый конец. В пробирке бурно выделяется газообразный ацетилен.
Химизм процесса:
СаС2 + 2Н2О → НС≡СН + Са(ОН)2
Поджигают ацетилен у конца газоотводной трубки. Он горит светящимся, коптящим пламенем. Реакция взаимодействия карбида кальция с водой экзотермична.
Ацетилен, полученный из карбида кальция, содержит незначительные количества NH3, РН3, АsН3 и других примесей и поэтому имеет характерный запах. Примеси можно удалить промыванием ацетилена водным раствором дихромата калия, подкисленного серной кислотой.
Опыт 2. Присоединение к ацетилену брома.
Реактивы и материалы: ацетилен; бромная вода, насыщенный раствор. Оборудование: газоотводная трубка.
Добавляют в пробирку с карбидом кальция (см. опыт 1) еще 2 капли воды и закрывают ее пробкой с газоотводной трубкой, коней которой опускают в пробирку с 5 каплями бромной воды. Бромная вода обесцвечивается вследствие присоединения атомов брома по месту тройной связи.
Химизм процесса:
НС≡СН + 2Вr2 → CHBr2–СНВr2
1,1,2,2-тетрабромэтан
Опыт 3. Отношение ацетилена к окислителям.
Реактивы и материалы: ацетилен; перманганат калия, 0,1 н. раствор. Оборудование: газоотводная трубка.
В пробирку помещают 1 каплю перманганата калия и 4 капли воды. В пробирку с кусочками карбида кальция добавляют еще 2 капли воды и закрывают пробкой с газоотводной трубкой, конец которой опускают в приготовленный раствор перманганата калия.
Розовый раствор быстро обесцвечивается: происходит окисление ацетилена по месту разрыва тройной связи с образованием промежуточного продукта окисления – щавелевой кислоты, которая окисляется дальше до диоксида углерода:
НС≡СН + 4 → HO – C – C – OH → 2CO2 + H2O
|| ||
O O
щавелевая кислота
Обесцвечивание бромной воды и раствора перманганата калия доказывает непредельность ацетилена.
Опыт 4. Образование ацетиленида серебра.
Реактивы и материалы: ацетилен; нитрат серебра, 0,2 н. раствор; аммиак, концентрированный раствор.
В пробирку вносят 2 капли раствора нитрата серебра и прибавляют 1 каплю раствора аммиака – образуется осадок гидроксида серебра. При добавлении 1-2 капель раствора аммиака осадок AgOH легко растворяется с образованием аммиачного раствора оксида серебра (OH).
Через аммиачный раствор оксида серебра пропускают ацетилен (см. опыт 1). В пробирке образуется светло-желтый осадок ацетиленида серебра, который затем становится серым.
Химизм процесса:
НС≡СН + 2ОН → AgС≡СAg↓ + 4NH3+ 2Н2О
Опыт 5. Образование ацетиленида меди.
Реактивы и материалы: карбид кальция; хлорид меди CuCl2, аммиачный раствор. Оборудование: фильтровальная бумага (полоски размером 5*40 мм).
В сухую пробирку помещают 1-2 кусочка карбида кальция и добавляют 2 капли воды. В отверстие пробирки вводят полоску фильтровальной бумаги, смоченной аммиачным раствором хлорида меди CuCl2, содержащим комплексный аммиакат состава C12. Появляется красно-бурое окрашивание вследствие образования ацетиленида меди.
В водных растворах ацетилениды серебра и меди устойчивы. В сухом состоянии при нагревании или при ударе они взрываются с большой силой.
Химизм процесса:
НС≡СН + 2C1 → CuС≡СCu↓ + 2NH4Cl + 2NH3
Литература:
1. Аверина А.В., Снегирева А.Я. Лабораторный практикум по органической химии. М.: Высшая школа, 1980. – С. 31-33.
Лабораторная работа №5
Ароматические углеводороды.
Цель: экспериментальное получение и изучение свойств ароматических углеводородов.
⇐ Предыдущая5Следующая ⇒
Рекомендуемые страницы:
Гибридные атомные орбитали ацетилена
Углерод в возбужденном состоянии содержит три р-орбитали и одну s с неспаренными электронами. При образовании метана (СН4) они принимают участие в создании равноценных связей с атомами водорода. Известный американский исследователь Л. Полинг разработал учение о гибридном состоянии атомных орбиталей (АО). Объяснение поведения углерода в химических реакциях заключается в выравнивании АО по форме и энергии, образовании новых облаков. Гибридные орбитали дают более прочные связи, становится устойчивее формула.
Атомы углерода в молекуле ацетилена, в отличие от метана, подвергаются sp-гибридизации. По форме и энергии смешиваются s- и р электроны. Появляются две sp-орбитали, лежащие под углом 180°, направленные по разные стороны от ядра.